pH7属于中性。在探讨液体的化学属性时,pH值是一个关键指标,用于描述溶液的酸碱性。这个概念在化学、生物学、环境科学乃至日常生活中都有广泛的应用。

pH值的基本定义
pH值是一个衡量溶液酸碱度的数值标准,其范围从0到14。这一度量标准基于溶液中氢离子(实际上是水合氢离子[H3O+])的活度(在稀溶液中可以近似视为浓度)。pH值的计算公式是pH = -log[H+],其中[H+]表示溶液中的氢离子浓度,单位为摩尔每升(mol/L)。
pH7的特殊意义
当pH值等于7时,这表明溶液是中性的,即其中的氢离子浓度和氢氧根离子浓度相等。这一点在纯水或中性溶液中尤其明显,因为纯水中[H+]和[OH-]的浓度均为1×10^-7 mol/L,使得其pH值正好为7。因此,在标准条件下(即298K或25°C下),pH值为7的溶液被定义为中性,既不是酸性也不是碱性。

酸性和碱性溶液的pH值
溶液的pH值如果小于7,则表示溶液是酸性的,这意味着溶液中的氢离子浓度超过了氢氧根离子浓度。相反,如果pH值大于7,则溶液是碱性的,其中的氢氧根离子浓度高于氢离子浓度。因此,pH值提供了一种量化溶液酸碱性强度的方法。
pH值的测量及其重要性
pH值的测量对于多种科学研究和工业应用至关重要。它不仅可以帮助科学家理解化学反应的性质,还对水质监测、食品安全、药物制造等领域有着重要的影响。通过精确测量pH值,可以确保环境和产品的安全性和稳定性。
pH值在不同条件下的变化
值得注意的是,在非水溶液或非标准温度和压力条件下,pH=7可能不再代表溶液呈中性。这是因为溶剂的电离常数在不同条件下会发生变化,从而影响中性pH值的具体数值。例如,在100°C的温度下,水的自偶电离平衡发生变化,使得中性溶液的pH值接近6而非7。
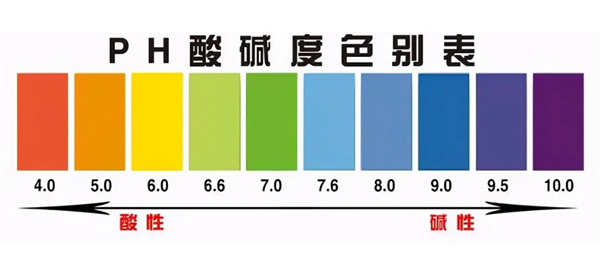
pH值是判断溶液酸碱性的关键指标,而pH值为7的溶液在标准条件下被定义为中性,既不偏酸也不偏碱。然而,环境条件的变化会影响到pH值与溶液性质的关系,这要求在实际应用中需要对这些变量保持警惕。通过深入理解pH值的含义和测量方法,我们可以更好地掌握化学反应的本质,优化工业过程,保护环境安全,并提高生活质量。






